Trên hành tinh chúng ta, các nguyên tố hóa học được sắp xếp sử dụng một hệ thống gọi là “bảng tuần hoàn”. Điều này giúp chúng ta hiểu được tính chất và cấu trúc của từng nguyên tố. Trong bài viết này, chúng ta sẽ tìm hiểu về lý thuyết bảng tuần hoàn các nguyên tố hóa học.
- Cách dùng và nghĩa của “Xếp Loại Học Lực” trong tiếng Anh: Định nghĩa, Ví dụ Anh-Việt
- Bộ 200 Đề thi Vật Lí 10 năm 2023: Ôn tập hiệu quả, đạt điểm cao!
- Tạo bộ font chữ tập viết Tiểu học để luyện viết tiếng Việt đơn giản và dễ dàng
- Bài test tiếng Anh cho học sinh lớp 2: Kết quả nhanh, chính xác
- Tổng hợp 1500 từ vựng tiếng Anh thông dụng theo chủ đề
Nguyên tắc sắp xếp các nguyên tố hóa học
Các nguyên tố hóa học được sắp xếp trên bảng tuần hoàn dựa trên các nguyên tắc sau:
Bạn đang xem: Lý thuyết bảng tuần hoàn các nguyên tố hóa học: Hiểu rõ sắp xếp các nguyên tố hóa học
- Các nguyên tố được xếp theo chiều tăng dần của điện tích hạt nhân.
- Các nguyên tố có cùng số lớp electron trong nguyên tử sẽ được xếp vào cùng hàng ngang (chu kì).
- Các nguyên tố có cùng số electron hóa trị sẽ được xếp vào cùng một cột nhóm.
Cấu tạo bảng tuần hoàn các nguyên tố hóa học
1. Ô nguyên tố
Số thứ tự của ô nguyên tố trên bảng tuần hoàn bằng số hiệu nguyên tử của nguyên tố đó. Đồng nghĩa với việc số e (electron), số p (proton) và số điện tích hạt nhân là như nhau. Dưới đây là hình minh họa:
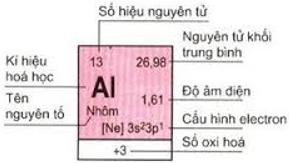
2. Chu kì và nhóm
a) Chu kì
- Chu kì là dãy các nguyên tố có cùng số lớp electron, được xếp theo chiều tăng dần điện tích hạt nhân.
- Số thứ tự của chu kì trùng với số lớp electron ở nguyên tử các nguyên tố trong chu kì đó.
- Chu kì nhỏ gồm chu kì 1, 2, 3 và chu kì lớn gồm chu kì 4, 5, 6, 7.
Ví dụ: Mg (magnesium) có cấu trúc electron là 1s²2s²2p⁶3s², nên nó thuộc chu kì 3 vì có 3 lớp electron.
b) Nhóm nguyên tố
- Nhóm nguyên tố là tập hợp các nguyên tố có cấu trúc electron tương tự nhau, giúp chúng có tính chất hóa học gần giống nhau và được xếp vào cùng một cột.
- Có 2 loại nhóm nguyên tố là nhóm A (bao gồm nguyên tố s và p) và nhóm B (bao gồm nguyên tố d và f).
- Số thứ tự của nhóm A bằng tổng số electron ở lớp ngoài cùng.
- Số thứ tự của nhóm B tuân theo công thức (x + y)B, trong đó (x + y) là tổng số electron cuối cùng (trong phân lớp d và f).
- Đặc biệt, nếu (x + y) = 3 → 7, nguyên tố thuộc nhóm (x + y)B; nếu (x + y) = 8 → 10, nguyên tố thuộc nhóm VIIIB; nếu (x + y) > 10, nguyên tố thuộc nhóm (x + y – 10)B.
Khối các nguyên tố
- Khối các nguyên tố s: gồm các nguyên tố nhóm IA và IIA. Đây là những nguyên tố mà electron cuối cùng trong nguyên tử sẽ điền vào phân lớp s.
- Khối các nguyên tố p: gồm các nguyên tố từ nhóm IIIA đến VIIIA (trừ He). Đây là những nguyên tố mà electron cuối cùng trong nguyên tử sẽ điền vào phân lớp p.
- Khối các nguyên tố d: gồm các nguyên tố thuộc nhóm B. Đây là những nguyên tố mà electron cuối cùng trong nguyên tử sẽ điền vào phân lớp d.
- Khối các nguyên tố f: gồm các nguyên tố thuộc họ Lantan và họ Actini. Đây là những nguyên tố mà electron cuối cùng trong nguyên tử sẽ điền vào phân lớp f.
Dưới đây là sơ đồ tư duy về bảng tuần hoàn các nguyên tố hóa học:
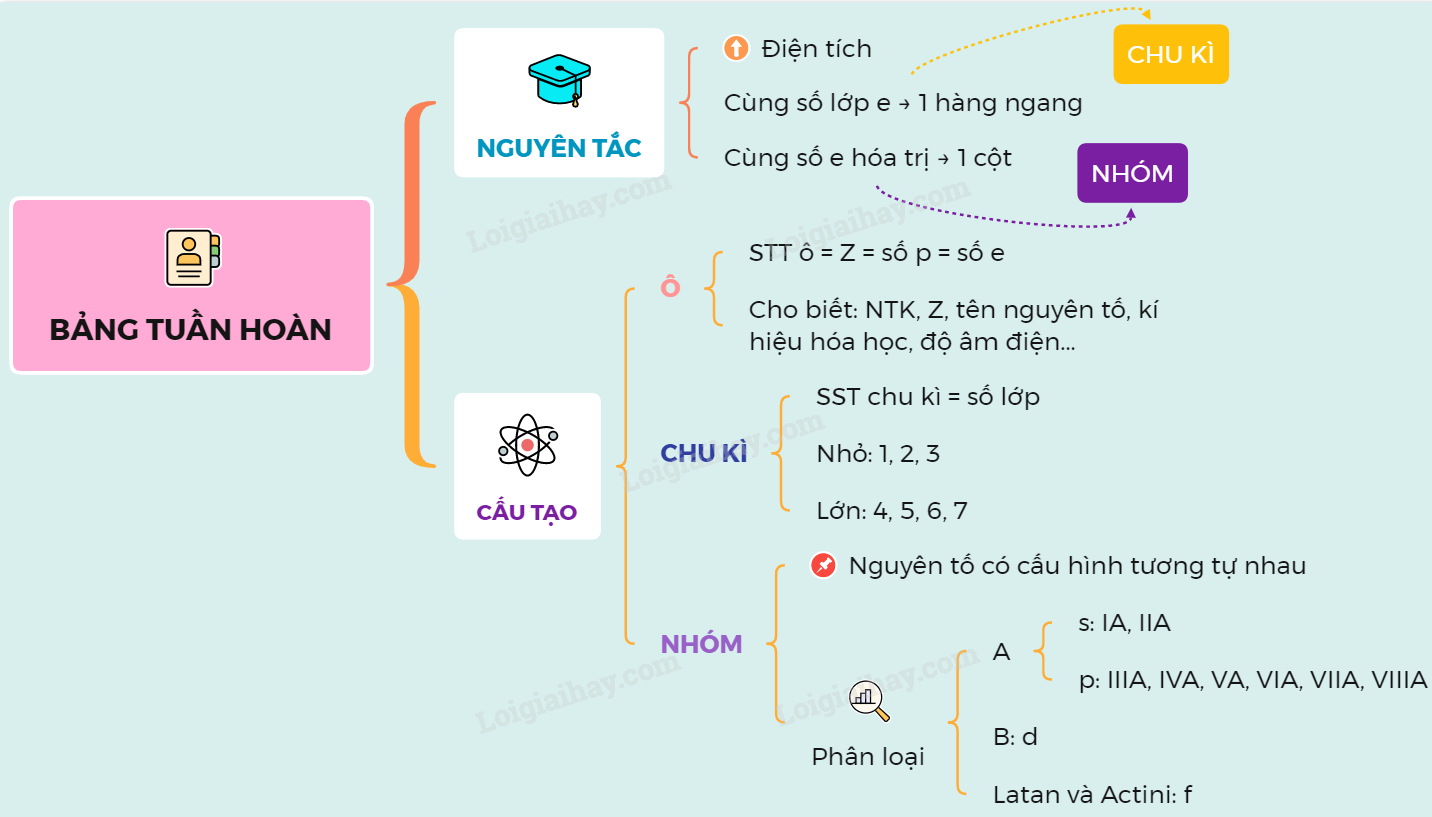
Thông qua lý thuyết bảng tuần hoàn các nguyên tố hóa học, chúng ta có thể hiểu rõ hơn về sự sắp xếp và cấu trúc của các nguyên tố. Điều này giúp chúng ta nắm bắt được các tính chất và ứng dụng của từng nguyên tố trong lĩnh vực hóa học. Hy vọng bài viết đã giúp các bạn hiểu rõ hơn về lý thuyết bảng tuần hoàn các nguyên tố hóa học.
Nguồn: Loigiaihay.com
Nguồn: https://thuysi.edu.vn
Danh mục: Giáo Dục